行业动态
本土药企、跨国药企政策跟进能力大
作者: 来源:神宇医药 日期:2015-04-21 09:25:00
“加快品种”
目前暂无相关政策发布,从CDE标记有“加快品种”的产品看,疫苗占较大比例
至于“加快品种”,目前暂无相关政策发布。“加快品种”的政策主要是推进临床亟需仿制药优先审评制度建设。传说中有62个仿制药进行优先审评,但究竟是哪62个还是云里雾里。
从目前CDE标记有“加快品种”的产品来看,疫苗占了较大比例,如脊髓灰质炎相关疫苗、H7N9流感病毒相关疫苗、十三价肺炎球菌疫苗、麻疹疫苗、风疹疫苗等。
政策跟进能力PK
进口企业VS国内企业
三大通道吻合度:诺华NO.1,恒瑞NO.2,辉瑞NO.3
那么,“重大专项”、“特殊审批”和“加快品种”的注册受理号是否都属于国产厂家呢?
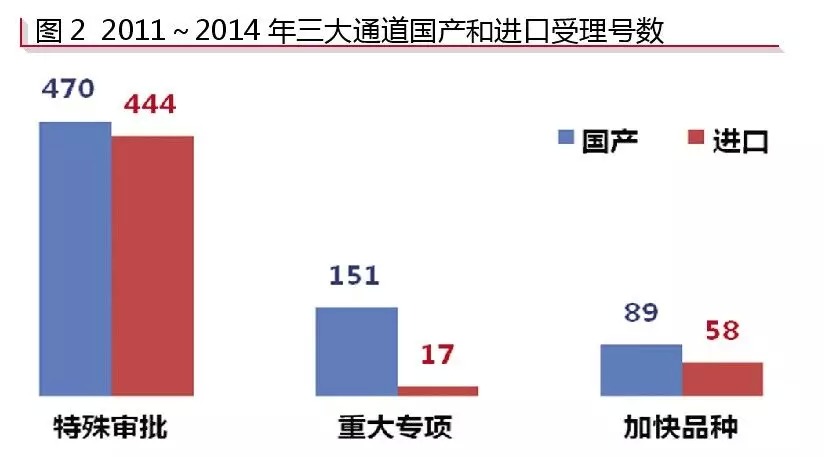
根据咸达数据V3.1的监测,“特殊审批”中,进口药品注册申报的较多,占比为48.58%,共444条受理号,其中97.97%为申报临床;“特殊审批”中,申报生产的国产受理号与进口受理号之比约为5:1;“加快品种”中,国产受理号与进口受理号之比为89:59;“重大专项”则更偏向于国产受理号,国产受理号与进口受理号的比约为9:1(见图2)。
一家企业如果能够非常娴熟地运用“重大专项”、“特殊审批”和“加快品种”等政策去申报注册产品,虽然未必能代表其创新能力,但一定能说明其非常适应国家的创新药鼓励政策。

如表1所示,三大通道受理号最多的生产企业是诺华,其次是恒瑞,第三位是辉瑞。前十一排名中,5个是国产企业,6个是进口企业。若不考虑“特殊审批”申报临床的数据,那么排名第一的是恒瑞,其次是豪森和天坛生物,第三是拜耳。
以上数据表明,实际响应国内创新药政策的国内企业并不多。相较于国内企业,国外企业更积极去适应国内的新药政策,以使自己的产品尽快上市。
国内企业开始觉醒
一季度,国内企业“特殊审批”提速,是进口企业的4倍
2011~2014年,恒瑞的受理号(除备案)共346条,属于三大通道的受理号共63条,占整体受理号数的18.21%;豪森的受理号(除备案)共299条,属于三大通道的受理号共63条,占整体受理号数的17.72%。
相较而言,同期科伦的受理号(除备案)共635条,但只有2个受理号属于“特殊审批”,且申报的是临床,尚无“重大专项”和“加快品种”的受理号。齐鲁受理号数为448条,有8个受理号属于“特殊审批”的临床申请,亦无“重大专项”和“加快品种”的受理号。科伦的申报受理号数是恒瑞的1.8倍,但恒瑞在三大通道的受理号数是科伦的32倍。
最近传闻,药品审批速度要加快了,以往积压的药品注册申请问题有望3年解决。假如产品批文获批速度加快,那么接下来就要开始面对多家生产企业的药品招标议价降价问题。在一众政策山雨欲来风满楼的层层压力之下,国内生产企业越来越关注创新药及其配套政策。
过去4年,国内生产企业实际申报的产品与国家三大通道政策的吻合度,远远不及进口企业。国内企业申报产品的策略更倾向于市场策略,应付招标政策。
可喜的是,国内企业已认识到变革迫在眉梢。2015年第一季度,国产企业“特殊审批”受理号数量是进口企业的4倍,这或许是我国创新药春天到来的一个信号。
提问:
国内完全自主研发的创新药有多少?
根据咸达数据V3.1,2014年1.1类化药9个受理号获批生产,涉及4个化学通用名,其中包括“阿德福韦酯”;3.1类化药70个受理号获批生产,5类26条,6类222条。2013年,1.1类获批的新药化药受理号有4个,涉及2个化学通用名,也包括“阿德福韦酯”,还有“帕拉米韦三水合物”;同年3.1类化药获批受理号95条,5类25条,6类223条。
若按照真正意义上的新化合物是我国自主研发才算创新药,那么我国的创新药和仿制药的比例恐怕会远低于1:100。